HDAC6 抑制剂
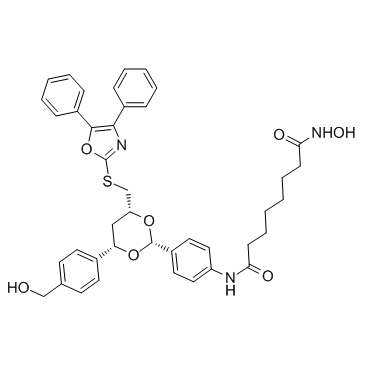
HDAC6 抑制剂结构式

|
常用名 | HDAC6 抑制剂 | 英文名 | Tubacin |
|---|---|---|---|---|
| CAS号 | 537049-40-4 | 分子量 | 721.861 | |
| 密度 | 1.3±0.1 g/cm3 | 沸点 | N/A | |
| 分子式 | C41H43N3O7S | 熔点 | N/A | |
| MSDS | 美版 | 闪点 | N/A |
HDAC6 抑制剂用途Tubacin 是一种有效的,选择性的 HDAC6 抑制剂,IC50 值为 4 nM,大约是对 HDAC1 的 350 倍。 |
||||
HDAC6 抑制剂作用体外活性:不直接稳定微管的Tubacin诱导α-微管蛋白乙酰化增加,A549细胞中EC50为2.5μM。 Tubacin抑制HDAC6介导的α-微管蛋白去乙酰化,并抑制野生型和HDAC6过表达细胞的迁移。 Tubacin与紫杉醇联合,可协同增强微管蛋白乙酰化。 Tubacin显着抑制药物敏感性和耐药性MM细胞生长,IC50为5-20μM,并通过激活半胱天冬酶诱导细胞凋亡。体内活性:在鸡胚中,Tubacin对HDAC6活性的抑制减少了基质胶/尼龙网中新血管的形成。 在植入小鼠的血管反应器中,Tubacin也会损害新血管的形成。 |
| 中文名 | HDAC6 抑制剂 |
|---|---|
| 英文名 | Octanediamide, N1-[4-[(2R,4R,6S)-4-[[(4,5-diphenyl-2-oxazolyl)thio]methyl]-6-[4-(hydroxymethyl)phenyl]-1,3-dioxan-2-yl]phenyl]-N8-hydroxy-, rel |
| 英文别名 | 更多 |
| 描述 | Tubacin 是一种有效的,选择性的 HDAC6 抑制剂,IC50 值为 4 nM,大约是对 HDAC1 的 350 倍。 |
|---|---|
| 相关类别 | |
| 靶点实验 |
HDAC6:4 nM (IC50) HDAC3:1.27 μM (IC50) HDAC8:1.27 μM (IC50) HDAC1:1.40 μM (IC50) HDAC5:3.35 μM (IC50) HDAC10:3.71 μM (IC50) HDAC11:3.79 μM (IC50) HDAC9:4.31 μM (IC50) HDAC2:6.27 μM (IC50) HDAC7:9.70 μM (IC50) HDAC4:17.30 μM (IC50) |
| 体外研究 | Tubacin优先诱导浓度为2.5μM的α-微管蛋白高度乙酰化,并诱导5μM的α-微管蛋白乙酰化,并通过过氧化还原酶乙酰化[1]保护前列腺癌(LNCaP)细胞免受过氧化氢诱导的8μM死亡[1]。 Tubacin(2.5和5μM)特异性诱导MM细胞中α-微管蛋白的乙酰化。 Tubacin显着抑制药物敏感性和耐药性MM细胞生长,72小时IC50为5-20μM。 Tubacin还通过激活半胱天冬酶诱导细胞凋亡。此外,Tubacin抑制HDAC6与动力蛋白的结合,并且当与硼替佐米组合时,其诱导多泛素化蛋白的显着积累。 Tubacin和硼替佐米在MM细胞系中诱导协同抗肿瘤活性,并抑制旁分泌MM细胞生长。 Tubacin(5μM)协同增强硼替佐米诱导的患者MM细胞的细胞毒性,对PBMC无细胞毒性[2]。 Tubacin可以浓度依赖性地抑制JEV诱导的细胞病变效应和细胞凋亡,以及降低人小脑成神经管细胞瘤细胞中的病毒产量。 Tubacin的病毒产量IC50为0.26μM。 Tubacin还有意义地阻止细胞内感染性病毒颗粒的产生,IC50为1.52μM。 Tubacin诱导HDAC6底物Hsp90的高度乙酰化,并减少Hsp90与JEV NS5蛋白的相互作用[3]。 |
| 细胞实验 | 在测定中使用HDAC抑制剂TSA,VPA,tubacin和TBSA。通过MTT(3-(4,5-二甲基噻唑-2-基)-2,5-二苯基溴化四唑)测定评估HDACi对TE671和BHK-21细胞的细胞毒性。将每孔5×104个细胞接种在96孔板中,然后用指定浓度的每种HDACi处理。处理48小时后,向每个孔中加入25μLMTT溶液(5mg / mL)并在37℃下用5%CO 2温育3小时。用磷酸盐缓冲盐水(PBS)洗涤三次后,向每个孔中加入100μLDMSO以溶解甲crystals晶体。通过micro-ELISA读数器测量OD570-630并计算存活率以指示每种HDACi对TE671和BHK-21细胞存活的抑制作用。存活率(%)=((Acontrol - Aexperiment)/ Acontrol)×100%。通过计算机程序[3]计算50%细胞毒性浓度(CC50)值。 |
| 参考文献 |
| 密度 | 1.3±0.1 g/cm3 |
|---|---|
| 分子式 | C41H43N3O7S |
| 分子量 | 721.861 |
| 精确质量 | 721.282166 |
| PSA | 168.45000 |
| LogP | 5.82 |
| InChIKey | BHUZLJOUHMBZQY-YXQOSMAKSA-N |
| SMILES | O=C(CCCCCCC(=O)Nc1ccc(C2OC(CSc3nc(-c4ccccc4)c(-c4ccccc4)o3)CC(c3ccc(CO)cc3)O2)cc1)NO |
| 外观性状 | white to tan |
| 折射率 | 1.668 |
| 储存条件 | ?20°C |
| 水溶解性 | DMSO: ≥10mg/mL |
| 危险品运输编码 | NONH for all modes of transport |
|---|
|
SMAR1 coordinates HDAC6-induced deacetylation of Ku70 and dictates cell fate upon irradiation.
Cell Death Dis. 5 , e1447, (2014) Acetylation status of DNA end joining protein Ku70 dictates its function in DNA repair and Bax-mediated apoptosis. Despite the knowledge of HDACs and HATs that are reported to modulate the acetylation... |
|
|
Limited efficacy of specific HDAC6 inhibition in urothelial cancer cells.
Cancer Biol. Ther. 15(6) , 742-57, (2014) Epigenetic modifiers such as histone deacetylases (HDACs) have come into focus as novel drug targets for cancer therapy due to their functional role in tumor progression. Since common pan-HDAC inhibit... |
|
|
Syntheses and discovery of a novel class of cinnamic hydroxamates as histone deacetylase inhibitors by multimodality molecular imaging in living subjects.
Cancer Res. 74(24) , 7475-86, (2014) Histone deacetylases (HDAC) that regulate gene expression are being explored as cancer therapeutic targets. In this study, we focused on HDAC6 based on its ability to inhibit cancerous Hsp90 chaperone... |
| UNII:02C2G1D30D |
| N-(4-{(2R,4R,6S)-4-{[(4,5-Diphenyl-1,3-oxazol-2-yl)sulfanyl]methyl}-6-[4-(hydroxymethyl)phenyl]-1,3-dioxan-2-yl}phenyl)-N'-hydroxyoctanediamide |







