105558-26-7
| 中文名 | 人参皂苷 Rh3 |
|---|---|
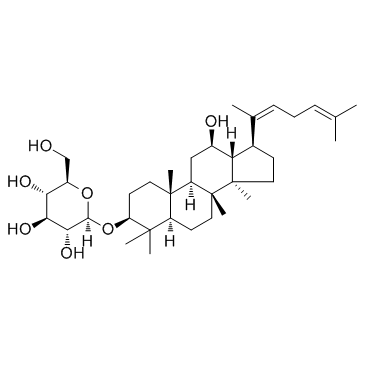
| 英文名 | (2R,3S,4S,5R,6R)-2-(hydroxymethyl)-6-[[(8R,10R,12S,13R,14S,17S)-12-hydroxy-4,4,8,10,14-pentamethyl-17-[(2Z)-6-methylhepta-2,5-dien-2-yl]-2,3,5,6,7,9,11,12,13,15,16,17-dodecahydro-1H-cyclopenta[a]phenanthren-3-yl]oxy]oxane-3,4,5-triol |
| 中文别名 |
人参皂苷 S-RH3
人参皂苷RH3 |
| 英文别名 |
(3β,12β,20Z)-12-Hydroxydammara-20(22),24-dien-3-yl β-D-glucopyranoside
β-D-Glucopyranoside, (3β,12β,20Z)-12-hydroxydammara-20(22),24-dien-3-yl GinsenosideRh3 N1608 Ginsenoside Rh3 |
| 描述 | Ginsenoside Rh3 是 Ginsenoside Rg5 的一种细菌代谢产物。在人视网膜细胞中 Ginsenoside Rh3 可诱导 Nrf2 激活。 |
|---|---|
| 相关类别 | |
| 靶点 |
Nrf2[1] |
| 体外研究 | 人参皂苷Rh3通过激活核因子E2相关因子2(Nrf2)信号传导抑制紫外线诱导的视网膜细胞氧化损伤。视网膜细胞中的人参皂苷Rh3处理诱导Nrf2活化。测试人参皂甙Rh3对视网膜色素上皮细胞(RPE)中Nrf2信号传导的潜在活性。 qRT-PCR测定结果表明,用人参皂苷Rh3处理剂量依赖性地增加mRNA转录和关键Nrf2调节基因的表达,包括HO1,NQO1和GCLC。因此,这些Nrf2依赖性基因(HO1,NQO1和GCLC)的蛋白质表达在人参皂苷Rh3(3-10μM)处理的RPE中也显着增加。值得注意的是,尽管人参皂甙Rh3处理后Nrf2 mRNA水平没有变化,但其Rh3蛋白水平显着增加[1]。 EZ-Cytox测定用于评估人参皂苷-Rh3对SP1-角质形成细胞活力的影响。人参皂苷Rh3(0.01,0.1,1和10μM)在所有浓度下均未显示出细胞毒性[2]。 |
| 体内研究 | 使用光诱导的视网膜损伤模型检查人参皂甙Rh3的潜在作用。人参皂甙Rh3玻璃体内注射(5mg/kg体重,30分钟预处理)显着减弱光诱导的a波和b波振幅的降低。视网膜电图(ERG)的a波在光照下降至对照水平的46.03±1.62%,在人参皂苷Rh3给药后恢复至71.84±7.51%。通过光照射,b波为对照水平的40.19±3.34%,并且Rh3玻璃体内注射回到对照水平的80.01±2.37%[1]。 |
| 细胞实验 | 将SP-1角质形成细胞接种在96孔板(2×10 4细胞/孔)中。 24小时后,用含有各种浓度的(A)SKRG或(B)人参皂苷Rh3(0.01,0.1,1和10μM)的培养基替换培养基。用DMSO处理对照细胞,终浓度为0.1%。 24小时后,含有化合物或DMSO的培养基用含有10%EZ-Cytox的培养基替换。然后将细胞在37℃下孵育1小时,并使用酶标仪在450nm的波长下测量吸光度。所有测定均一式三份进行[2]。 |
| 动物实验 | 小鼠[1]使用BALB / c小鼠(雄性,5-6周龄,17-18g重量)。在暴露于5000lx的白色荧光之前进行瞳孔扩张。在光照前30分钟,将人参皂甙Rh3(5mg / kg体重)玻璃体内注射到右眼。曝光后的ERG记录也是早期报道的。从a波的波谷到b波的峰值测量b波振幅,并且从初始基线测量a波的振幅。 |
| 参考文献 |
| 密度 | 1.2±0.1 g/cm3 |
|---|---|
| 沸点 | 695.0±55.0 °C at 760 mmHg |
| 分子式 | C36H60O7 |
| 分子量 | 604.857 |
| 闪点 | 374.1±31.5 °C |
| 精确质量 | 604.433899 |
| PSA | 119.61000 |
| LogP | 7.10 |
| 蒸汽压 | 0.0±4.9 mmHg at 25°C |
| 折射率 | 1.570 |
| 储存条件 | 2-8℃ |
| 危险品运输编码 | NONH for all modes of transport |
|---|