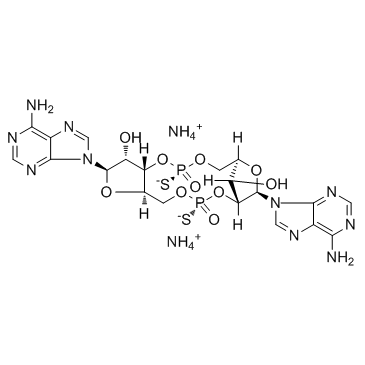
1638750-96-5
| 中文名 | ADU-S100铵盐 |
|---|---|
| 英文名 | ML RR-S2 CDA ammonium salt |
| 英文别名 |
(1R,6R,8R,9R,10S,15S,17R,18S)-8,17-Bis(6-amino-9H-purin-9-yl)-3,12-disulfanyl-2,4,7,11,13,16-hexaoxa-3,12-diphosphatricyclo[13.2.1.06,10]octadecane-9,18-diol 3,12-dioxide diammoniate
ML RR-S2 CDA (ammonium salt) |
| 描述 | ADU-S100 ammonium salt 是干扰素基因刺激物的激活剂 (STING)。 |
|---|---|
| 相关类别 | |
| 靶点 |
STING[1] |
| 体外研究 | ADU-S100在THP-1人单核细胞中显示出比CDA增强的I型IFN产生。相反,dithio,混合连接环二核苷酸(CDN)衍生物(ML RR-CDA,ML RR-S2 CDG和ML RR-S2 cGAMP)有效激活所有五个hSTING等位基因,包括难治性hSTINGREF和hSTINGQ等位基因。与内源性ML cGAMP和TLR3激动剂poly I:C相比,ADU-S100以摩尔当量为基础诱导IFN-β和促炎细胞因子TNF-α,IL-6和MCP-1的最高表达。还发现ADU-S100诱导STING的聚集并诱导小鼠骨髓巨噬细胞(BMM)中TBK1和IRF3的磷酸化。与ML cGAMP相比,ADU-S100诱导显着更高水平的IFN-α[1]。 |
| 体内研究 | ADU-S100显示出比内源性ML cGAMP更高的抗肿瘤控制。 ADU-S100化合物的剂量反应在B16荷瘤小鼠中进行,该小鼠确定了最佳抗肿瘤剂量水平,同时引发最大肿瘤抗原特异性CD8 + T细胞反应,并将长期存活率提高至50%[1] 。 |
| 细胞实验 | 将冷冻保存的hPBMC解冻,将每孔1×10 6个细胞接种于96孔板中的RPMI培养基中,所述培养基补充有10%FBS,1%非必需氨基酸,1%青霉素/链霉素,L-谷氨酰胺,10mM HEPES缓冲液, 1mM丙酮酸钠,0.055mMβ-ME,37℃,5%CO 2。用10μMADU-S100或ML cGAMP刺激细胞6小时,收获上清液。将上清液1:2稀释,并使用Cytometric Bead Array(CBA)Human Flex Set测定IFN-α蛋白。使用FACSVerse细胞计数器收集数据并通过FCAP阵列软件[1]分析。 |
| 动物实验 | 小鼠[1] WT C57BL / 6小鼠在左侧腹侧接种5×104个B16.F10细胞(n = 8)。当肿瘤体积为100mm 3时,小鼠接受三个IT剂量的ML RR-S2 CDG(25μg),ADU-S100(50μg)或HBSS作为对照。 WT C57BL / 6小鼠在左胁腹(n = 5)中接种5×104 B16.F10细胞。当肿瘤体积为100mm 3时,他们接受3剂量的ADU-S100,剂量为5,25,50或100μg或HBSS作为对照。 WT C57BL / 6小鼠在左侧腹侧接种5×104个B16.F10细胞(n = 8)。当肿瘤体积为100mm 3时,它们接受三个IT剂量的100μgADU-S100或HBSS作为对照。在第13,17和20天施用治疗,并且每周两次进行肿瘤测量。结果显示为Log-rank(Mantel-Cox)测试(A和C)的存活百分比。 |
| 参考文献 |
| 分子式 | C20H30N12O10P2S2 |
|---|---|
| 分子量 | 724.604 |
| 精确质量 | 724.112427 |
| 储存条件 | -20°C,密闭,干燥 |