| 描述 |
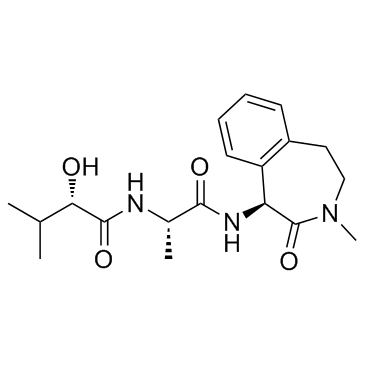
Semagacestat 是一种 γ-secretase 抑制剂,抑制 β-amyloid (Aβ42),Aβ38 和 Aβ40,IC50 分别为 10.9,12 和 12.1 nM。也抑制 Notch,IC50 为 14.1 nM。
|
| 相关类别 |
|
| 靶点实验 |
IC50: 10.9 nM (Aβ42), 12 nM (Aβ38), 12.1 nM (Aβ40), 14.1 nM (Notch)[1]
|
| 体外研究 |
Semagacestat(LY450139)可以减少96孔培养基中Aβ42,Aβ40和Aβ38的分泌,并且如预期的那样增加细胞裂解液中的β-CTF,尽管这种增加在高浓度时出乎意料地减弱[1]。在皮质神经元(CTX)中,Semagacestat(LY450139)引起分泌到培养基中的Aβ40浓度依赖性降低,Semagacestat的IC50值为111 nM。 Semagacestat引起分泌到培养基中的Aβ40和Aβ42浓度依赖性降低,IC50值分别为126和130 nM [2]。
|
| 体内研究 |
发现Semagacestat(LY450139)以10 mg/kg降低Aβ42和Aβ40(降低22-23%; p <0.01),并以剂量依赖性方式增加β-CTF(0.3-10 mg/kg)(15-162) %升高; 1-10 mg/kg时p <0.01)[1]。 γ-分泌酶抑制剂Semagacestat(LY450139)是一种高效低分子量化合物,可显着降低永久过表达APP的细胞培养物中的β-淀粉样蛋白(Aβ)水平,以及野生型和转基因APP表达小鼠。与载体处理的对照相比,在野生型C57BL/6小鼠的脑中,给药30mg/kg后3小时的Semagacestat水平的Aβ40减少了43%(未配对t检验,p = 0.002)。皮下注射Semagacestat(30 mg/kg)可暂时降低透析液中Aβ40的含量,给药后3小时Aβ40水平最大降低80%(p <0.001)[2]。
|
| 激酶实验 |
将稳定过表达人野生型APP695的H4人神经胶质瘤细胞维持在补充有10%胎牛血清和青霉素/链霉素的DMEM中。将细胞在96孔或6孔板中培养过夜,然后用各种浓度的每种药物(例如,Semagacestat)处理24小时。使用单独的ELISA试剂盒测量培养基中Aβ1-42,Aβ1-40和Aβ1-38的水平。为了量化β-CTF,用含有完全蛋白酶抑制剂混合物的RIPA缓冲液(25mM Tris,150mM NaCl,1%NP-40,1%脱氧胆酸钠,0.1%SDS; pH 7.6)裂解细胞并应用于人β -CTF ELISA试剂盒,1:20稀释。细胞裂解物的等分试样也用于CellTiter-Glo发光细胞活力测定。将来自六孔板的细胞裂解物进行Western印迹分析[1]。
|
| 细胞实验 |
从第14天至第16天胎儿C57BL / 6小鼠分离鼠皮质神经元(CTX)。简言之,将解离的神经元以0.25×10 6个细胞/ cm 2(800000个细胞/ mL;100μL/孔,96孔板)的密度接种在100μg/ mL聚-L-赖氨酸包被的培养皿上,并在补充的Neurobasal培养基中培养。含2%B-27补充剂,不含抗氧化剂,0.5 mM L-谷氨酰胺和100 U / mL青霉素和0.1 mg / mL链霉素。通过更换一半培养基每三天喂食神经元。通过针对神经胶质原纤维酸性蛋白的抗体评估,培养物中神经胶质细胞的比例小于10%。在完全培养基更换后,在体外6天(DIV)使用CTX,并与分泌酶抑制剂(例如,Semagacestat)一起温育24小时。在DIV 7使用神经元和细胞培养基。为了检测细胞活力,通过它们在用0.5mg / mL MTT孵育60分钟后降低MTT的能力来定量活细胞的百分比。在所有体外药理学实验后,常规测量活力[2]。
|
| 动物实验 |
小鼠[1]使用表达具有瑞典突变(K670N / M671L)的人APP695的雌性Tg2576小鼠。获得雄性转基因小鼠并与雌性B6SJLF1 / J小鼠杂交。为了识别药物对认知功能的影响,进行了四种不同的实验。实验1的目的是阐明急性和亚慢性药物对Tg2576小鼠认知缺陷的影响。将每种药物(Semagacestat,BMS-708163和GSM-2)口服给予5.5个月大的Tg2576小鼠8天。在第1天和第8天给药后3小时进行Y-迷宫测试以评估空间工作记忆。载体处理的Tg2576小鼠在Y-迷宫测试中表现出比WT小鼠显着更低的自发交替率,表明空间工作记忆缺陷。在第1天,1mg / kg Semagacestat,1mg / kg BMS-708163和0.1-0.3mg / kg GSM-2显着改善这些认知缺陷(急性效应)。然而,在第8天,GSI效应消失,而GSM-2保留其显着效应(亚慢性效应)。在第8天Y-迷宫测试后立即杀死小鼠,此时通过ELISA测定Aβ42,Aβ40和β-CTF的海马水平。
|
| 参考文献 |
[1]. Mitani Y, et al. Differential effects between γ-secretase inhibitors and modulators on cognitive function in amyloid precursor protein-transgenic and nontransgenic mice. J Neurosci. 2012 Feb 8;32(6):2037-50. [2]. Elvang AB, et al. Differential effects of gamma-secretase and BACE1 inhibition on brain Abeta levels in vitro and in vivo. J Neurochem. 2009 Sep;110(5):1377-87. [3]. Justice NJ, et al. Posttraumatic stress disorder-like induction elevates β-amyloid levels, which directly activates corticotropin-releasing factor neurons to exacerbate stress responses. J Neurosci. 2015 Feb 11;35(6):2612-23. [4]. Portelius E, et al. Acute effect on the Aβ isoform pattern in CSF in response to γ-secretase modulator and inhibitor treatment in dogs. J Alzheimers Dis. 2010;21(3):1005-12.
|