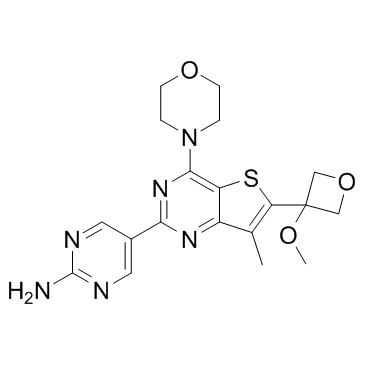
| 描述 |
GNE-317 是一种 PI3K/mTOR 抑制剂,能够穿过血脑屏障 (BBB)。
|
| 相关类别 |
|
| 靶点 |
PI3K
mTOR
|
| 体外研究 |
GNE-317是GDC-0980的氧杂环丁烷衍生物,其合成目的是降低外排转运蛋白的底物亲和力。在体外,GDC-0980和GNE-317在使用GL261细胞系的MTS细胞毒性实验中表现出相似的特征[1]。
|
| 体内研究 |
在用GL261-GFP-Luc细胞接种后7天,每天用最大耐受剂量的GDC-0980(7.5mg/kg),GNE-317(30mg/kg)或载体处理小鼠一次。对于GL261,通过每周一次的生物发光成像跟踪肿瘤生长。在3组中GL261肿瘤生长没有显着变化。在评估GL261的存活益处时,GDC-0980和GNE-317均未提供超过载体处理的动物的存活益处。这些药物在体内无效的事实由体外细胞毒性数据表明,该药物在GL261细胞系中诱导细胞死亡的效力有限。尽管GNE-317具有更高的递送和增强的治疗靶向功效,但这两种药物在GL261肿瘤中均无效[1]。
|
| 细胞实验 |
GL261是一种侵袭性C57BL / 6J衍生的神经胶质瘤系。用来自不同质粒的绿色荧光蛋白(GFP)和荧光素酶(Luc)转染该细胞系。将得到的单克隆GL261-GFP-Luc细胞维持在补充有10%FBS和青霉素/链霉素(100U / mL)的Dulbecco改良的Eagle培养基中,并在5%氧气下培养。细胞选择使用4mg / mL嘌呤霉素和4mg / mL G418。细胞活力测定以96孔格式建立,在培养条件下每孔接种2000个细胞。将细胞在药物或载体存在下孵育48小时,并通过MTS测定评估活力。使用Synergy Mx自动读板仪,使用490nm处的吸光度来确定活力,并使用650nm处的吸光度来考虑背景。将药物处理的孔的数值标准化为载体处理的孔的值,以产生存活百分比[1]。
|
| 动物实验 |
将小鼠[1] GL261-GFP-Luc细胞植入7周龄的C57BL / 6J小鼠中。当肿瘤达到5e7光子/ s / cm2 / sr(辐射)时,动物口服给予最大耐受剂量的GDC-0980(7.5mg / kg),GNE-317(30mg / kg)或载体,每天一次,持续3天。最大耐受剂量定义为体重下降<10%的小鼠可施用的最大剂量。即使在这些不同剂量下,两种剂量都提供相似的血浆浓度,因此提供相同的总体全身暴露。在第三次给药后1或6小时,用二氧化碳使小鼠安乐死并用30mL PBS灌注。借助GFP护目镜,将大脑切割成肿瘤核心,肿瘤边缘和正常脑组织。处理组织样品和血液,并使用LC-MS / MS分析来自每组的组织样品的药物浓度。
|
| 参考文献 |
[1]. Salphati L, et al. Distribution of the phosphatidylinositol 3-kinase inhibitors Pictilisib (GDC-0941) and GNE-317 in U87 and GS2 intracranial glioblastoma models-assessment by matrix-assisted laser desorption ionization imaging. Drug Metab Dispos. 2014 Jul;42(7):1110-6. [2]. Becker CM, et al. Decreased affinity for efflux transporters increases brain penetrance and molecular targeting of a PI3K/mTOR inhibitor in a mouse model of glioblastoma. Neuro Oncol. 2015 Sep;17(9):1210-9.
|