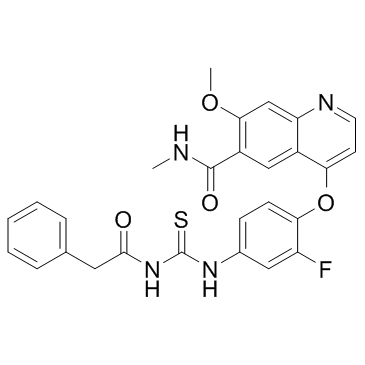
| 描述 |
TAS-115 是一种有效的 VEGFR 和 c-Met/HGFR 抑制剂,能够抑制 rVEGFR2 和 rMET 的活性,IC50 值分别为 30 和 32 nM。
|
| 相关类别 |
|
| 靶点 |
VEGFR2:30 nM (IC50)
c-Met:32 nM (IC50)
|
| 体外研究 |
TAS-115是ATP拮抗剂,其抑制常数(Ki)值分别对rVEGFR2和rMET为12和39nM。 AS-115与其他已知的VEGFR或MET抑制剂一样强烈抑制VEGFR2和MET的激酶活性及其信号依赖性细胞生长。与其他VEGFR抑制剂相比,TAS-115对各种正常细胞的损伤较小[1]。 TAS-115在浓度低于10μM时不影响PC-9或HCC827细胞的生长;然而,TAS-115与厄洛替尼的组合使用以浓度依赖性方式逆转HGF诱导的细胞系抗性。 TAS-115抑制癌细胞产生VEGF和内皮细胞增殖[2]。
|
| 体内研究 |
TAS-115(50mg/kg/d)在治疗期间完全阻止肿瘤生长。 TAS-115(200mg/kg/d)诱导MET扩增的人癌移植模型中初始肿瘤体积的48%回归。该模型中TAS-115的估计50%有效剂量(ED50)为8mg/kg/d。当以50或200mg/kg/d的剂量给药时,TAS-115显着延长这些小鼠的存活[1]。 TAS-115在体内抑制PC-9/HGF肿瘤中的血管生成。此外,双重厄洛替尼和TAS-115成功抑制PC-9/HGF肿瘤生长,并延迟肿瘤再生与肿瘤血管抑制持续相关,即使停止治疗后[2]。
|
| 激酶实验 |
使用迁移率变动分析进行酶抑制研究。简而言之,0.3μg/ mL重组MET(rMET,N-末端谷胱甘肽S-转移酶(GST)标签)和1.5μMFL-肽2或2μg/ mL重组VEGFR2(rVEGFR2,氨基酸790-末端,N -minminal 6His Tagged)和1.5μM的FL-Peptide 22加入25μL含有1/2米氏常数(Km)ATP水平,100 mM HEPES(pH 7.2),0.003%(w / v)的混合物中。 Brij35,0.04%(v / v)吐温20,10mM MgCl 2,1mM二硫苏糖醇,完全不含EDTA的小型蛋白酶抑制剂鸡尾酒片和PhosSTOP磷酸酶抑制剂鸡尾酒片,加入0.05%(w / v)仅在rVEGFR2的情况下CHAPSO。将反应混合物在28℃下温育90分钟,并通过加入15mM EDTA终止反应。使用LabChip EZ Reader,版本2.1.82.0(UCC版本:1.96,CCD版本:102)计算磷酸化肽。基于在对照孔和药物处理孔中形成的磷酸化肽的量,使用逻辑回归分析计算50%抑制浓度(IC 50)。使用ProfilerPro试剂盒1-8进行总共192次激酶组测定,并使用迁移率变动分析进行分析。
|
| 细胞实验 |
使用MTT染料还原法测量细胞生长。将肿瘤细胞以2×103细胞/ 100mL RPMI-1640培养基的密度接种到96孔板中,每孔含10%FBS。孵育24小时后,向各孔中加入各种试剂,将细胞再培养72小时,然后向各孔中加入50μLMTT溶液(2mg / mL)并孵育2小时。除去含有MTT溶液的培养基,加入100mL二甲基亚砜溶解深蓝色晶体。用酶标仪在测试和参考波长分别为550和630nm下测量每个孔的吸光度。显示相对于未处理对照的生长百分比。在每个实验期间,每种试剂浓度至少一式三份进行测试,并且每个实验至少进行三次。
|
| 动物实验 |
通过套管针将SC-9片段皮下植入每只小鼠的右腹部。制备MKN45细胞的悬浮液并皮下植入每只裸鼠的右腹部。计算肿瘤体积(TV,mm3)。 TAS-115剂量水平设定为12.5,50和200mg / kg / d。舒尼替尼的剂量水平设定为40 mg / kg / d;该剂量相当于最大耐受剂量(MTD)。对于SC-9异种移植模型中的慢性给药,口服药物治疗持续连续14或42天。在治疗期间,每周测量两次电视和体重。
|
| 参考文献 |
[1]. Fujita H, et al. The novel VEGF receptor/MET-targeted kinase inhibitor TAS-115 has marked in vivo antitumor properties and a favorable tolerability profile. Mol Cancer Ther. 2013 Dec;12(12):2685-96. [2]. Nakade J, et al. Triple inhibition of EGFR, Met, and VEGF suppresses regrowth of HGF-triggered, erlotinib-resistant lung cancer harboring an EGFR mutation. J Thorac Oncol. 2014 Jun;9(6):775-83.
|