人参皂苷Rg1
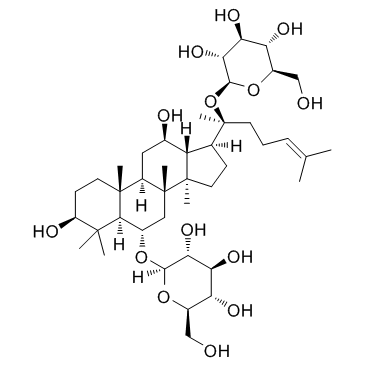
人参皂苷Rg1结构式

|
常用名 | 人参皂苷Rg1 | 英文名 | Ginsenoside Rg1 |
|---|---|---|---|---|
| CAS号 | 22427-39-0 | 分子量 | 801.013 | |
| 密度 | 1.3±0.1 g/cm3 | 沸点 | 898.5±65.0 °C at 760 mmHg | |
| 分子式 | C42H72O14 | 熔点 | 194~197 ℃ | |
| MSDS | 中文版 美版 | 闪点 | 497.2±34.3 °C | |
| 符号 |

GHS07 |
信号词 | Warning |
人参皂苷Rg1用途Ginsenoside Rg1 是人参的主要活性成分之一。Ginsenoside Rg1 通过降低大脑 Aβ 水平来发挥作用。Ginsenoside Rg1 减少 NF-κB 核易位。 |
| 中文名 | 人参皂苷 Rg1 |
|---|---|
| 英文名 | ginsenoside Rg1 |
| 中文别名 | 人参皂苷Rg1 | 人参皂荚RG1 | 人参皂苷Rg1 |
| 英文别名 | 更多 |
| 描述 | Ginsenoside Rg1 是人参的主要活性成分之一。Ginsenoside Rg1 通过降低大脑 Aβ 水平来发挥作用。Ginsenoside Rg1 减少 NF-κB 核易位。 |
|---|---|
| 相关类别 | |
| 靶点实验 |
Aβ1-42 p65 |
| 体外研究 | 人参皂苷Rg1促进人牙髓细胞(hDPCs)的增殖和分化。 hDPCs在人参皂苷Rg1中的增殖能力显着增强(p <0.05),尤其是在人参皂苷Rg1(5μM)组中。与对照组相比,诱导组,人参皂苷Rg1组及其联合组的DSPP和DMP1的ALP活性和基因表达均增加(p <0.05)[3]。在由脂多糖(LPS)刺激的RAW264.7细胞中,p-IκBα和p-p65的水平显着高于对照,并且PPAR-γ水平显着降低。用Rg1体外处理抑制IκBα磷酸化,减少NF-κB核转位并上调PPAR-γ表达[2]。 |
| 体内研究 | 在佐剂诱导的关节炎(AIA)大鼠的发炎关节中,p-IκBα和p-p65的水平显着高于对照,并且PPAR-γ水平显着降低。人参皂甙Rg1体内抑制可抑制IκBα磷酸化,减少NF-κB核转位,上调PPAR-γ表达[2]。与阿尔茨海默病(AD)模型组相比,人参皂苷Rg1(G-Rg1)和人参皂苷Rg2(G-Rg2)在最后两个训练日减少逃避潜伏期(p <0.05)。在空间探索测试中,在AD模型组小鼠中,在目标象限中花费的总时间和完全越过平台的先前位置的小鼠的数量分别明显更短和更低(正常对照组小鼠)( p <0.01),通过用人参皂苷Rg1和人参皂苷Rg2(人参皂苷Rg1,p <0.01;人参皂苷Rg2,p <0.05)处理而逆转的趋势。用人参皂苷Rg1和人参皂苷Rg2治疗有效地改善了由于AD导致的小鼠的认知功能。人参皂苷Rg1和人参皂苷Rg2减少APP/PS1小鼠中的Aβ1-42积累。在人参皂苷Rg1和人参皂苷Rg2处理的小鼠中,在APP/PS1小鼠中观察到的病理学异常逐渐改善。清晰的核仁和浅棕色,稀疏分散的Aβ沉积物是可见的[1]。 |
| 细胞实验 | 将hDPC与不同浓度的人参皂苷Rg1(0.1,0.5,2.5,5,10和20μM)一起温育。人参皂甙Rg1对hDPCs增殖能力的影响通过成纤维细胞集落形成试验,MTT试验和流式细胞术评估细胞周期。设计对照组,成骨诱导组,人参皂苷Rg1(5μM)组和联合组,碱性磷酸酶(ALP)活性和FQ-PCR检测牙本质涎磷蛋白(DSPP)和牙本质基质蛋白1(DMP1)的基因表达。进行评估hDPCs的分化[3]。 |
| 动物实验 | 小鼠[1]使用体重20±2g的雄性APP / PS1小鼠和体重20±2g的雄性C57BL / 6J小鼠。将动物保持在空气动物中心中,温度为23±2℃,相对湿度为50±10%,具有自然的光 - 暗循环。食物和水可随意提供。适应1周后,将小鼠分成4组(每组n = 10):正常对照组,AD模型组,人参皂苷Rg1组和人参皂苷Rg2组。根据浓度 - 反应曲线,人参皂苷Rg1和人参皂苷Rg2组中的小鼠每天腹膜内注射人参皂苷Rg1和人参皂苷Rg2(30mg / kg),溶于盐水中。用等剂量盐水(0.9%w / v)处理AD模型组(APP / PS1小鼠)和正常对照组(C57BL / 6J非转基因同窝小鼠)中的小鼠。在脑代谢物分析之前,将所有小鼠处理1个月。 |
| 参考文献 |
| 密度 | 1.3±0.1 g/cm3 |
|---|---|
| 沸点 | 898.5±65.0 °C at 760 mmHg |
| 熔点 | 194~197 ℃ |
| 分子式 | C42H72O14 |
| 分子量 | 801.013 |
| 闪点 | 497.2±34.3 °C |
| 精确质量 | 800.492188 |
| PSA | 239.22000 |
| LogP | 1.66 |
| InChIKey | YURJSTAIMNSZAE-HHNZYBFYSA-N |
| SMILES | CC(C)=CCCC(C)(OC1OC(CO)C(O)C(O)C1O)C1CCC2(C)C1C(O)CC1C3(C)CCC(O)C(C)(C)C3C(OC3OC(CO)C(O)C(O)C3O)CC12C |
| 外观性状 | 白色结晶粉末 |
| 蒸汽压 | 0.0±0.6 mmHg at 25°C |
| 折射率 | 1.602 |
| 储存条件 | |
| 稳定性 | |
| 分子结构 | 1、 摩尔折射率:205.93 2、 摩尔体积(cm3/mol):600.3 3、 等张比容(90.2K):1717.9 4、 表面张力(dyne/cm):67.0 5、 极化率(10-24cm3):81.63 |
| 计算化学 | 1、疏水参数计算参考值(XlogP):2.7 2、氢键供体数量:10 3、氢键受体数量:14 4、可旋转化学键数量:10 5、互变异构体数量: 6、拓扑分子极性表面积(TPSA):239 7、重原子数量:56 8、表面电荷:0 9、复杂度:1390 10、同位素原子数量:0 11、确定原子立构中心数量:0 12、不确定原子立构中心数量:22 13、确定化学键立构中心数量:0 14、不确定化学键立构中心数量:0 15、共价键单元数量:1 |
| 更多 | 1.性状:白色结晶粉末。 2.密度(g/mL,25/4℃):未确定 3.相对蒸汽密度(g/mL,空气=1):未确定 4.熔点(ºC):194-196.5 5.沸点(ºC,常压):未确定 6.沸点(ºC,5.2kPa):未确定 7.折射率:未确定 8.闪点(ºC):未确定 9.比旋光度(º):未确定 10.自燃点或引燃温度(ºC):未确定 11.蒸气压(kPa,25ºC):未确定 12.饱和蒸气压(kPa,60ºC):未确定 13.燃烧热(KJ/mol):未确定 14.临界温度(ºC):未确定 15.临界压力(KPa):未确定 16.油水(辛醇/水)分配系数的对数值:未确定 17.爆炸上限(%,V/V):未确定 18.爆炸下限(%,V/V):未确定 19.溶解性:溶于乙醇。 |
| 符号 |

GHS07 |
|---|---|
| 信号词 | Warning |
| 危害声明 | H302 |
| 警示性声明 | P301 + P312 + P330 |
| 个人防护装备 | dust mask type N95 (US);Eyeshields;Gloves |
| 危害码 (欧洲) | Xn: Harmful; |
| 风险声明 (欧洲) | R22 |
| 安全声明 (欧洲) | 2-45 |
| 危险品运输编码 | UN 1230 3/PG 2 |
| WGK德国 | 3.0 |
| RTECS号 | LY9537200 |
|
~% 
人参皂苷Rg1 22427-39-0 |
| 文献:EP2570132 A2, ; Paragraph 0049; 0050; 0051 ; |
|
~% 
人参皂苷Rg1 22427-39-0 |
| 文献:Zou, Kun; Zhu, Shu; Tohda, Chihiro; Cai, Shaoqing; Komatsu, Katsuko Journal of Natural Products, 2002 , vol. 65, # 3 p. 346 - 351 |
|
~% 
人参皂苷Rg1 22427-39-0 |
| 文献:Planta Medica, , vol. 69, # 3 p. 285 - 286 |
| 人参皂苷Rg1上游产品 2 | |
|---|---|
| 人参皂苷Rg1下游产品 3 | |
|
Transcriptome analysis of Panax vietnamensis var. fuscidicus discovers putative ocotillol-type ginsenosides biosynthesis genes and genetic markers.
BMC Genomics 16 , 159, (2015) P. vietnamensis var. fuscidiscus, called "Yesanqi" in Chinese, is a new variety of P. vietnamensis, which was first found in Jinping County, the southern part of Yunnan Province, China. Compared with ... |
|
|
[Cultivation of Panax ginseng adventitious roots in bubble bioreactors].
Zhongguo Zhong Yao Za Zhi 37(24) , 3706-11, (2012) To study cultivation of Panax ginseng adventitious roots in bubble bioreactors.The adventitious roots were obtained through tissue culture different types of bioreactors. The contents of ginsenosides ... |
|
|
Th1 immunity induction by ginsenoside Re involves in protection of mice against disseminated candidiasis due to Candida albicans.
Int. Immunopharmacol. 14(4) , 481-6, (2012) Type-1 and -2 responses of T helper lymphocytes demonstrate essentially different and opposite effector functions. In the present study, we determined the immunoregulatory effect of ginsenoside Re aga... |
| (2R,3R,4S,5S,6R)-2-({(3S,5R,6S,8R,9R,10R,12R,13R,14R,17S)-3,12-Dihydroxy-4,4,8,10,14-pentaméthyl-17-[(2S)-6-méthyl-2-{[(2S,3R,4S,5S,6R)-3,4,5-trihydroxy-6-(hydroxyméthyl)tétrahydro-2H-pyran-2-yl]oxy}-5-heptèn-2-yl]hexadécahydro-1H-cyclopenta[a]phénanthrén-6-yl}oxy)-6-(hydroxyméthyl)tétrahydro-2H-pyran-3,4,5-triol |
| GINSENOSIDE RGL |
| PANAXOSIDE A |
| Ginsenoside Rg1 |
| EINECS 244-989-9 |
| MFCD00210293 |
| ginsenoside-Rg2 |
| (3β,6α,12β)-20-(β-D-Glucopyranosyloxy)-3,12-dihydroxydammar-24-en-6-yl β-D-glucopyranoside |
| panaxosiderg1 |
| (2R,3R,4S,5S,6R)-2-({(3S,5R,6S,8R,9R,10R,12R,13R,14R,17S)-3,12-Dihydroxy-4,4,8,10,14-pentamethyl-17-[(2S)-6-methyl-2-{[(2S,3R,4S,5S,6R)-3,4,5-trihydroxy-6-(hydroxymethyl)tetrahydro-2H-pyran-2-yl]oxy}-5-hepten-2-yl]hexadecahydro-1H-cyclopenta[a]phenanthren-6-yl}oxy)-6-(hydroxymethyl)tetrahydro-2H-pyran-3,4,5-triol |
| (3β,6α,12β)-20-(β-D-Glucopyranosyloxy)-3,12-dihydroxydammar-24-en-6-yl-β-D-glucopyranoside |
| Gensenoside Rg1 |
| ginsenosidea2 |
| GinsenosideRg1 |
| Rg1 |
| β-D-Glucopyranoside, (3β,6α,12β)-20-(β-D-glucopyranosyloxy)-3,12-dihydroxydammar-24-en-6-yl |
| SANCHINOSIDE C1 |
| ginsenosideg1 |
| ginsinoside Rg1 |

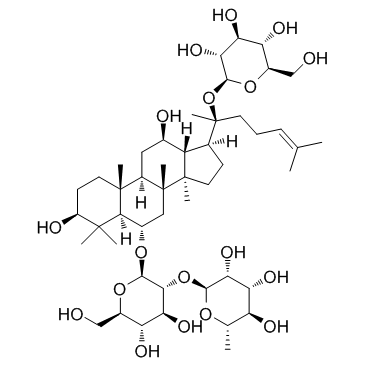
![6-O-[6-O-acetyl-β-D-glucopyranosyl]-20-O-(β-D-glucopyranosyl)-20(S)-protopanaxatriol结构式](https://image.chemsrc.com/caspic/253/163403-91-6.png)
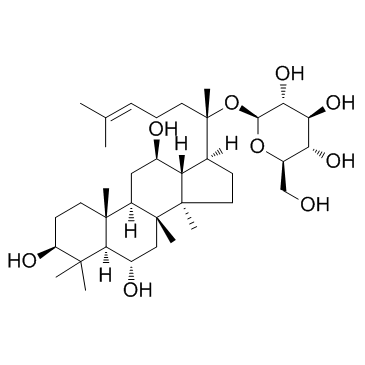 CAS号53963-43-2
CAS号53963-43-2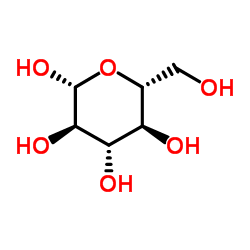 CAS号492-61-5
CAS号492-61-5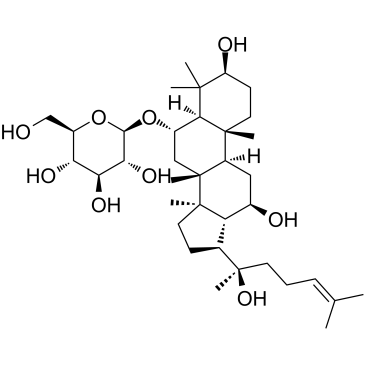 CAS号80952-71-2
CAS号80952-71-2





